Auteur:Équipe de R&D, arôme de Cuiguai
Publié par:Guangdong Unique Flavour Co., Ltd.
Last Updated: 16 janvier 2026

Tests de précision en laboratoire pour les e-liquides
Sur le marché très concurrentiel des e-liquides, la saveur est primordiale. Les fabricants investissent massivement dans le développement de profils de saveurs complexes et attrayants afin de fidéliser les consommateurs. Cependant, un défi courant et frustrant auquel sont confrontés les formulateurs est l'instabilité de la saveur, phénomène dans lequel un produit a un goût exceptionnel immédiatement après son mélange, mais se dégrade, mute ou s'estompe considérablement après des semaines en rayon.
Alors que beaucoup attribuent cela au vague concept de « trempage » ou de simple oxydation, un processus chimique plus insidieux en est souvent la cause :hydrolyse.
Pour les fabricants d’arômes spécialisés destinés à l’industrie du vapotage, comprendre l’hydrolyse n’est pas une simple chimie académique ; c'est un élément essentiel du contrôle de la qualité et de la viabilité du produit. Les e-liquides sont des matrices chimiques complexes contenant du propylène glycol (PG), de la glycérine végétale (VG), de la nicotine et des arômes. Bien que souvent considérée comme « anhydre » (sans eau), la réalité de la chimie des e-liquides est bien plus humide que beaucoup ne le pensent.
Cet article propose un examen technique détaillé de l’hydrolyse des esters dans le contexte des formulations d’e-liquides. Nous explorerons pourquoi les esters – l’épine dorsale des profils de saveurs fruitées et sucrées – sont vulnérables à la dégradation, le rôle catalytique de l’environnement du e-liquide et pourquoi les formulations « à base d’eau » présentent des défis de stabilité uniques.
Pour comprendre pourquoi la saveur se dégrade, nous devons d'abord comprendre quelle saveurestchimiquement. Alors que les arômes des e-liquides utilisent des alcools, des aldéhydes, des cétones et des terpènes, la grande majorité des notes fruitées, sucrées et dessertes proviennent deesters.
Les esters sont des composés organiques dérivés d'un acide (généralement un acide carboxylique) et d'un alcool. Ils sont omniprésents dans la nature, responsables des arômes vibrants de fruits et de fleurs. Dans l’industrie des arômes, ils sont synthétisés pour recréer ces expériences sensorielles.
Les exemples courants utilisés dans les e-liquides incluent :
Les esters sont choisis pour leur forte volatilité (leur permettant de se vaporiser facilement aux températures de vapotage) et leur puissant impact sensoriel. Cependant, la liaison chimique même qui forme un ester – la liaison ester – est également son talon d’Achille lorsqu’elle est introduite dans le mauvais environnement.
À la base, l’hydrolyse est une dégradation chimique due à une réaction avec l’eau. Le terme signifie littéralement « fractionnement de l’eau » (hydroélectrique= eau,lyse= déliement).
Dans le contexte des esters, l'hydrolyse est la réaction inverse de l'estérification. Lors de l'estérification, un alcool et un acide s'associent pour former un ester et créer de l'eau comme sous-produit. Lors de l'hydrolyse, l'eau attaque la liaison ester, la décomposant en son acide parent constitutif et son alcool parent.
L’équation chimique générale de l’hydrolyse des esters est la suivante :
R-COO-R' (Ester) + H₂O (Eau) ⇌ R-COOH (Acide carboxylique) + R'-OH (Alcool)
Où « R » et « R » représentent différents groupes alkyles (chaînes carbonées) qui définissent la molécule aromatique spécifique.
Cette réaction est un processus d’équilibre. Cela signifie que la réaction peut se dérouler dans les deux sens. Selon le principe de Le Chatelier, l’ajout de plus de réactif (dans ce cas, de l’eau) entraîne l’équilibre vers le produit (acide et alcool).
Lorsqu’un ester s’hydrolyse, la molécule aromatique souhaitée cesse d’exister. Elle est remplacée par deux nouvelles molécules, qui possèdent souvent des propriétés organoleptiques radicalement différentes et généralement indésirables.
Considérons l'hydrolyse deButyrate d'éthyle(note ananas):
La transformation est radicale. Une saveur tropicale vibrante ne s’estompe pas ; il s'aigre activement en raison de la formation d'acides carboxyliques. C’est pourquoi les e-liquides aux fruits vieillis ou mal formulés développent parfois des « notes désagréables » distinctes ou une morsure acide désagréable.
Comme indiqué dans les ressources fondamentales en chimie organique, bien que les esters soient généralement stables, leur liaison est susceptible d'être attaquée nucléophile par l'eau, en particulier lorsqu'elle est catalysée [1].
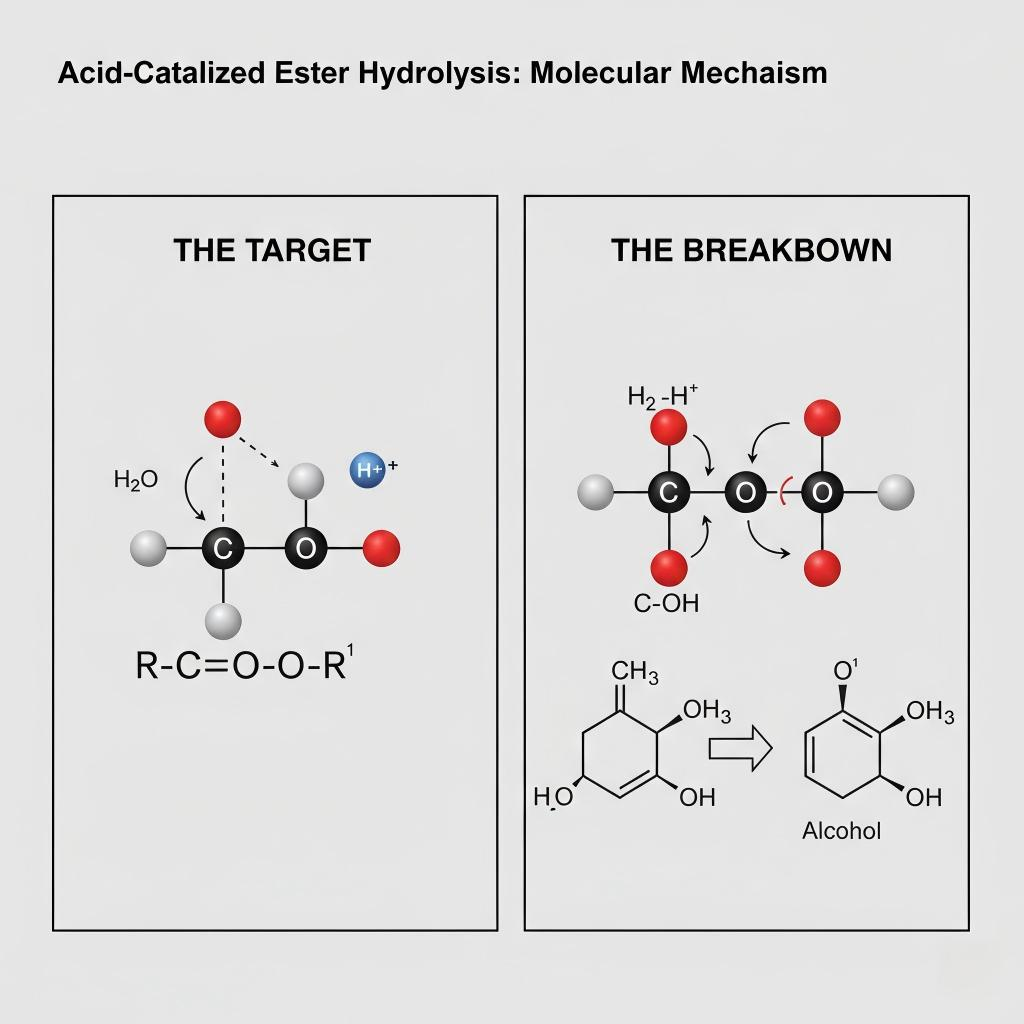
Diagramme d’hydrolyse des esters catalysés par l’acide
Si vous mélangez du butyrate d'éthyle pur avec de l'eau pure et neutre dans un bécher stérile à température ambiante, le taux d'hydrolyse sera extrêmement lent, probablement négligeable sur plusieurs mois. Les esters nécessitent une poussée pour se décomposer.
Malheureusement, l’environnement typique des e-liquides fournit plusieurs poussées puissantes, agissant comme des catalyseurs qui accélèrent considérablement cette réaction de dégradation.
Le réactif principal, l’eau, est presque toujours présent dans les e-liquides, même s’il n’est pas ajouté intentionnellement.
The presence of even 2-5% water in an e-liquid matrix is more than sufficient to shift the chemical equilibrium and drive the hydrolysis of sensitive flavor compounds.
L’accélérateur le plus important de l’hydrolyse des esters dans les e-liquides est l’acidité (pH faible). Le mécanisme réactionnel est très sensible à la concentration en ions hydrogène (H+).
Dans un environnement acide, un proton libre (H+) protonne l’oxygène carbonyle de l’ester. Cette étape rend le carbone carbonyle nettement plus électrophile (recherche de charge positive) et donc beaucoup plus vulnérable aux attaques de la molécule d'eau neutre (le nucléophile).
D'où vient l'acide dans les e-liquides ?
Les recherches en chimie alimentaire démontrent systématiquement que la stabilité des esters dépend fortement du pH, les taux d'hydrolyse augmentant de manière logarithmique à mesure que le pH s'écarte du neutre [2].
Comme la plupart des réactions chimiques, l’hydrolyse des esters dépend de la température, selon l’équation d’Arrhenius. L'augmentation de l'énergie thermique augmente l'énergie cinétique des molécules, conduisant à des collisions plus fréquentes et plus énergétiques, augmentant ainsi la vitesse de réaction.
Les e-liquides sont soumis à la chaleur lors de :
Pour le formulateur d’e-liquide, il est crucial de reconnaître que les différents esters ont une résistance différente à l’hydrolyse. Le taux de dégradation est régi par l'environnement stérique et électronique entourant la liaison ester.
L’encombrement stérique fait référence à « l’encombrement » physique de la molécule autour du site de réaction.
L'hydrolyse nécessite qu'une molécule d'eau accède physiquement au carbone carbonyle et l'attaque. Si l’ester possède de grandes chaînes carbonées volumineuses attachées à proximité de ce site, ces chaînes agissent comme un bouclier physique, bloquant l’approche de la molécule d’eau.
La nature électronique des groupes attachés à l'ester joue également un rôle. Les groupes qui retirent des électrons rendent le carbone carbonyle plus positif et plus attrayant pour l'eau (accélération de l'hydrolyse). Les groupes qui donnent des électrons stabilisent le carbonyle, ralentissant ainsi la réaction.
Un fabricant d’arômes qualifié ne choisit pas seulement un arôme en fonction de son odeur ; ils sélectionnent des molécules d'ester spécifiques en fonction de leur stabilité prévue au sein de la matrice PG/VG/Nicotine prévue.

Stabilité des e-liquides et tests de pH
Ne pas tenir compte des risques d’hydrolyse conduit à des produits qui échouent sur le marché. Les conséquences de la dégradation des esters sont tangibles et préjudiciables à la réputation de la marque.
L’impact le plus immédiat est une perte d’intensité sensorielle. Les notes de tête vibrantes (généralement les esters les plus petits, les plus volatils et les plus sujets à l'hydrolyse) disparaissent en premier. Un « mélange de fruits tropicaux » complexe peut se transformer en une douceur générique et plate à mesure que les molécules caractéristiques qui le définissent sont détruites.
Comme indiqué pour le butyrate d'éthyle, les produits de dégradation ont souvent mauvais goût. L'accumulation de divers acides carboxyliques (acétique, butyrique, valérique, propionique) conduit à des notes acides, fromagères, vinaigrées ou moites qui ruinent le profil recherché. Le produit n’a pas seulement un goût plus faible ; ça a le goûtfaux.
Des études menées dans l'industrie des boissons, qui partagent des défis similaires en matière de stabilité de la saveur, soulignent comment même des changements infimes dans les taux d'esters dus à l'hydrolyse peuvent considérablement altérer la qualité et la fraîcheur perçues d'un produit [3].
La génération d'acides carboxyliques lors de l'hydrolyse abaisse le pH du e-liquide au fil du temps. Cette « dérive du pH » peut avoir des effets secondaires. Si le pH descend trop bas, cela peut affecter la perception de la nicotine dans la gorge et potentiellement avoir un impact sur la stabilité des autres composés de la matrice.
Les magasins de vapotage et les distributeurs exigent des produits ayant une durée de conservation fiable (souvent 1 à 2 ans). Un e-liquide qui subit une hydrolyse importante dans les trois mois n’est pas viable commercialement. Cela entraîne des retours clients et des stocks morts.
Comprendre les risques de l’hydrolyse est la première étape vers sa prévention. En adoptant une approche de formulation axée sur la chimie, les fabricants peuvent prolonger considérablement la durée de conservation des produits et la fidélité des saveurs.
La stratégie la plus efficace consiste à priver la réaction de son réactif nécessaire : l’eau.
La gestion de l’acidité est cruciale, notamment avec les sels de nicotine.
C’est là que le partenariat avec un fabricant spécialisé d’arômes de vape devient essentiel. Une entreprise d’arômes alimentaires génériques peut fournir un arôme « Fraise » au goût excellent, conçu pour un produit de boulangerie au pH neutre et à courte durée de conservation. Cette même saveur peut échouer de manière catastrophique dans un e-liquide acide au sel de nicotine conservé pendant six mois.
Des fabricants spécialisés conçoivent des arômes pour l’environnement de la vape en :
La complexité de ces interactions chimiques souligne la nécessité de connaissances spécialisées en formulation d’e-liquides [4].
La création d’un e-liquide premium est un exercice d’équilibre entre art et science. Si l’art olfactif capte l’attention du client, c’est la science chimique qui garantit sa satisfaction durable.
L’hydrolyse des esters est une réalité chimique fondamentale dans les environnements aqueux et légèrement acides comme les e-liquides. L’ignorer entraîne une décoloration de la saveur, des notes désagréables et des produits instables. En comprenant les mécanismes de l'hydrolyse catalysée par l'acide, l'influence de la teneur en eau et la stabilité variable des différentes structures d'ester, les formulateurs peuvent prendre des décisions éclairées qui protègent l'intégrité de leurs profils aromatiques.
La stabilité n’est pas un accident ; il est conçu.

Vitrine de produits e-liquides haut de gamme
Ne laissez pas l’hydrolyse compromettre votre prochain e-liquide le plus vendu. ÀSaveur de cuiguai, nous ne créons pas seulement des saveurs ; nous les concevons pour résister aux défis chimiques uniques de l’environnement des e-liquides. Notre équipe de chimistes des arômes est spécialisée dans le développement de profils d’esters hautement stables optimisés pour les matrices PG/VG et les formulations de sels de nicotine.
Contactez-nous dès aujourd'hui pour une consultation technique ou pour demander des échantillons de nos arômes résistants à l'hydrolyse. Laissez-nous vous aider à formuler des produits qui ont aussi bon goût au 300e jour qu’au premier jour.
Contactez-nous:
| Canal de contact | Détails |
| 🌐 Site Internet : | www.cuiguai.com |
| 📧 E-mail : | informations@cuiguai.com |
| ☎ Téléphone : | +86 0769 8838 0789 |
| 📱WhatsApp : | +86 189 2926 7983 |
[1] Wikipédia. (s.d.). Hydrolyse. Récupéré dehttps://en.wikipedia.org/wiki/Hydrolyse[Consulté pour la définition chimique générale de l'hydrolyse des esters].
[2] Université de Calgary, Département de chimie. (s.d.). Hydrolyse d’ester catalysée par l’acide. Chem LibreTextes. Extrait de [Ressource éducative détaillant la cinétique et la dépendance au pH de l'hydrolyse].
[3] Parfumeur & Aromateur. (Divers problèmes). Stabilité de la saveur dans les bases de boissons acides. Médias d'affaires séduits. [Revue industrielle faisant référence aux défis de dégradation des arômes dans les environnements aqueux acides].
[4] Farsalinos, KE et al. (2014). Composition chimique des liquides des cigarettes électroniques et risque de dégradation des esters. [Une représentation générique de rapports de recherche spécifiques à l'industrie analysant la stabilité chimique des e-liquides].
La portée de l'entreprise comprend des projets agréés: la production d'additif alimentaire. Projets généraux: ventes d'additifs alimentaires; fabrication de produits chimiques quotidiens; ventes de produits chimiques quotidiens; services techniques, développement technologique, consultation technique, échange de technologie, transfert de technologie et promotion technologique; Recherche et développement des aliments biologiques; Recherche et développement de la préparation des enzymes industriels; cosmétiques en gros; agence de négociation nationale; ventes de produits sanitaires et de fournitures médicales jetables; Vétonnage des ustensiles de cuisine, des articles sanitaires et des tachages quotidiens; ventes de nécessités quotidiennes; Ventes alimentaires (uniquement les ventes de nourriture préemballée).
Copyright ©Guangdong Unique Flavour Co., Ltd.Tous droits réservés. politique de confidentialité